 22888840
22888840
 22888840
22888840
آنزیم محدودکننده یا Inhibitory Enzyme به آنزیمی اطلاق میشود که فعالیتش توسط یک محدودیت یا مهار کننده خاص محدود میشود. این محدودیت میتواند به صورت فیزیکی یا شیمیایی باشد و موجب کاهش یا مهار کامل فعالیت آنزیم میشود. آنزیم محدودکننده میتواند در فرایندهای زیستی مختلف از جمله سیگنالدهی سلولی، مسیرهای متابولیکی، و فرایندهای زیستی دیگر نقش داشته باشد.
این محدودیت معمولاً به عنوان یک کنترلگر طبیعی برای فعالیت آنزیمها عمل میکند و میتواند توسط سلولها برای تنظیم فعالیت فرایندهای زیستی استفاده شود. به عنوان مثال، در مسیرهای متابولیکی، فعالیت آنزیمها معمولاً توسط مواد شیمیایی آزمایشگاهی خاصی که به عنوان مهار کنندهها عمل میکنند، کنترل میشود. این محدودکنندهها میتوانند موادی مانند آنتیپروتئینها، مواد کمکی، یا تغییرات pH باشند.
استفاده از آنزیمهای محدودکننده میتواند در مطالعات زیستشناسی و بیوشیمیایی، در ساخت داروها و در تولید صنایع غذایی و دیگر صنایع مختلف مفید باشد. این آنزیمها اغلب به عنوان ابزارهای مهمی برای کنترل فعالیت آنزیمی و سیستمهای بیولوژیکی در مطالعات زیستشناسی مورد استفاده قرار میگیرند.
حتما بخوانید : آنتی بیوتیک آزمایشگاهی چیست ؟ کاربرد و انواع آن
ساختار و عملکرد آنزیمهای محدودکننده بسیار متنوع است و بسته به نوع آنزیم و محیط زیستی که در آن عمل میکنند، ممکن است متفاوت باشد. با این حال، این آنزیمها معمولاً به یکی از دو شیوه زیر عمل میکنند:
در این نوع مهار، آنزیم محدودکننده با یک یا چند عامل خارجی یا سوبسترات مشترک برای محصول میانی تشکیل شده ترکیب میکند و این ترکیب باعث مهار فعالیت آنزیم میشود. این نوع مهار ممکن است از نظر ساختاری معمولاً قابل مشاهده نباشد ولی در بسیاری از موارد تاثیر آن قابل لمس است.
در این نوع مهار، آنزیم محدودکننده بطور مستقیم با یک مولکول خاص ترکیب میشود و این ترکیب باعث مهار فعالیت آنزیم میشود. این نوع مهار معمولاً بر اساس تغییرات ساختاری در آنزیم و تغییرات در فعالیت کاتالیتیک آن رخ میدهد.
ساختار آنزیمهای محدودکننده متنوع است و میتواند شامل پروتئینها، آمینو اسیدها، نوکلئوتیدها و سایر مولکولهای بزرگ باشد. این آنزیمها ممکن است از یک یا چندین زمینه و فعالیت جایگزین بهره ببرند و از تغییرات در ساختار آنزیم یا محیط پیرامونی آن برای کنترل فعالیت آنزیمی استفاده کنند.
بیشتر بدانید : اسید آزمایشگاهی چیست؟ انواع رایج آن + کاربرد
عملکرد این آنزیمها معمولاً به یک یا چندین روش زیر بستگی دارد:
۱. تغییرات ساختاری: این آنزیمها میتوانند با تغییرات در ساختار آنزیم، به طور مستقیم فعالیت آنزیم را مهار کنند.
۲. رقابت با سوبسترات: این آنزیمها ممکن است با رقابت برای سوبسترات، موجب کاهش ترکیب آنزیم و سوبسترات شده و در نتیجه مهار فعالیت آنزیم را ایجاد کنند.
۳. تغییرات در محیط pH و دما: تغییرات در محیط زیستی مثل pH و دما میتواند به طور مستقیم بر فعالیت آنزیمها و ترکیب آنها تأثیر بگذارد و فعالیت آنها را مهار کند.
در کل، آنزیمهای محدودکننده نقش مهمی در تنظیم و کنترل فعالیت آنزیمها و فرآیندهای زیستی دارند و به عنوان ابزارهای مهمی در مطالعات زیستشناسی، بیوشیمی، داروسازی و صنایع مختلف به کار میروند
آنزیمهای محدودکننده بسیار متنوع هستند و میتوانند بر اساس نوع محدودیت و نوع آنزیم که مورد مهار قرار میگیرد، دستهبندی شوند. در زیر به برخی از انواع رایج آنزیمهای محدودکننده اشاره میشود:
این نوع مهارکنندهها به طور مستقیم با آنزیم ترکیب میشوند و فعالیت آنزیم را مهار میکنند. مثالهایی از این نوع شامل:
این نوع مهارکنندهها به طور غیر مستقیم با آنزیم ترکیب میشوند و تغییرات در ساختار سه بعدی آنزیم را ایجاد میکنند که منجر به مهار فعالیت آن میشود.
تغییرات در محیط pH میتواند به طور مستقیم بر فعالیت آنزیمها تأثیر بگذارد و فعالیت آنها را مهار کند.
تغییرات در دما نیز میتواند به طور مستقیم بر فعالیت آنزیمها تأثیر بگذارد و فعالیت آنها را مهار کند.
این نوع مهارکنندهها با تغییرات در ساختار آنزیم و انعطاف پذیری آن تأثیر مخربی دارند و فعالیت آن را مهار میکنند.
این نوع مهارکنندهها با کاهش بازده فرآیند آنزیمی، فعالیت آن را محدود میکنند.
این مولکولها با ترکیب با آنزیمها تعادل را به سمت مهار فعالیت آنزیم میکشانند.
مواد شیمیایی مختلفی میتوانند به عنوان مهارکنندههای آنزیمی عمل کنند و فعالیت آنزیمها را محدود کنند.
تعداد زیادی مهارکننده دیگر نیز وجود دارد که بر اساس مکانیسم و نوع اثرشان میتوانند دستهبندی شوند.
در کل، انواع آنزیمهای محدودکننده بسیار گسترده هستند و از طیف وسیعی از مکانیسمها و مولکولها برای مهار فعالیت آنزیمی استفاده میکنند.
آنزیم های محدود کننده به عنوان ابزارهای مولکولی قدرتمندی در مهندسی ژنتیک شناخته می شوند و نقشی اساسی در این علم ایفا می کنند. اهمیت این آنزیم ها را می توان در موارد زیر خلاصه کرد:
جداسازی ژن های مورد نظر از DNA موجودات زنده: آنزیم های محدود کننده با برش DNA در توالی های خاص، امکان جداسازی ژن های مورد نظر از سایر بخش های DNA را فراهم می کنند.
انتقال ژن به سلول های میزبان: پس از جداسازی، ژن ها می توانند با استفاده از آنزیم های محدود کننده به سلول های میزبان مانند باکتری ها یا سلول های گیاهی منتقل شوند.
بررسی ساختار ژن ها: آنزیم های محدود کننده برای برش DNA در مکان های مشخص و ایجاد الگوهای نواری قابل تجزیه و تحلیل توسط روش هایی مانند الکتروفورز ژل استفاده می شوند. این امر به دانشمندان در بررسی ساختار ژن ها و شناسایی نواحی عملکردی آنها کمک می کند.
تشخیص جهش ها و بیماری های ژنتیکی: با استفاده از آنزیم های محدود کننده می توان جهش ها و تغییرات در توالی DNA را که منجر به بیماری های ژنتیکی می شوند، شناسایی کرد.
ایجاد گیاهان و حیوانات تراریخته: با استفاده از آنزیم های محدود کننده می توان ژن های جدیدی را به DNA گیاهان و حیوانات وارد کرد و به آنها صفات جدیدی مانند مقاومت در برابر آفات یا بیماری ها، افزایش ارزش غذایی یا بهبود عملکرد تولیدی بخشید.
بررسی صحنه جرم و شناسایی مجرمان: آنزیم های محدود کننده برای تجزیه و تحلیل DNA موجود در صحنه جرم مانند خون، بزاق یا مو و مقایسه آن با نمونه های DNA مظنونین استفاده می شوند.
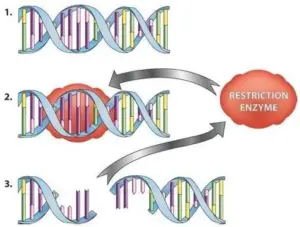

در مجموع، آنزیم های محدود کننده ابزارهای ضروری برای مهندسی ژنتیک و سایر زمینه های مرتبط با DNA هستند. این آنزیم ها به دانشمندان امکان می دهند ژن ها را دستکاری کرده، ساختار DNA را تجزیه و تحلیل کرده و organismos ترکیبی با ویژگی های جدید ایجاد کنند.
علاوه بر موارد ذکر شده، آنزیم های محدود کننده کاربردهای دیگری نیز در زمینه های مختلف علمی و تحقیقاتی دارند، از جمله:
با پیشرفت های مداوم در زمینه مهندسی ژنتیک، انتظار می رود که نقش آنزیم های محدود کننده در آینده حتی از این هم مهم تر شود.
مهندسی آنزیم های محدود کننده، فرآیندی جذاب و رو به پیش است که به دانشمندان امکان می دهد با دستکاری در ساختار و عملکرد این آنزیم های قدرتمند، ابزارهای مولکولی جدید و کارآمدتری برای تحقیقات ژنتیکی و کاربردهای مختلف ایجاد کنند.
شناسایی توالی های خاص: طراحی آنزیم هایی که می توانند توالی های منحصر به فرد و جدیدی از DNA را که قبلاً قابل شناسایی نبوده اند، شناسایی و برش دهند.
برش در مکان های دقیق: ایجاد آنزیم هایی که DNA را در مکان های دقیق تر و با ظرافت بیشتر برش می دهند تا کنترل و دقت بیشتری در مطالعات ژنتیکی و محصولات سیتوژنتیک به دست آید.
فعالیت در شرایط خاص: مهندسی آنزیم هایی که در شرایط extremophile مانند دمای بالا، pH بالا یا حضور مواد شیمیایی خاص فعال باشند و کاربردهای جدیدی را در زمینه های مختلف از جمله زیست فناوری صنعتی و پزشکی فراهم کنند.
بهبود کارایی: افزایش سرعت و کارایی آنزیم های محدود کننده برای انجام واکنش های برش DNA در مدت زمان کوتاه تر و با راندمان بالاتر.
کاهش خطا: کاهش احتمال خطا در فرآیند برش DNA توسط آنزیم های محدود کننده برای حصول نتایج دقیق تر و قابل اعتمادتر.
بیشتر بدانید : سیتوژنتیک چیست؟ انواع تکنیک های آن
جهش ژنی: معرفی جهش های هدفمند در ژن های کد کننده آنزیم های محدود کننده برای تغییر ساختار و عملکرد آنها.
ترکیب و جابجایی: ترکیب توالی های DNA از آنزیم های محدود کننده مختلف برای ایجاد آنزیم های جدید با ویژگی های ترکیبی.
طراحی منطقی: استفاده از روش های محاسباتی برای پیش بینی ساختار و عملکرد آنزیم های جدید و سپس سنتز آنها در آزمایشگاه.
تکامل هدایت شده: استفاده از فرآیندهای تکاملی آزمایشگاهی برای تکامل آنزیم های موجود با ویژگی های مطلوب.
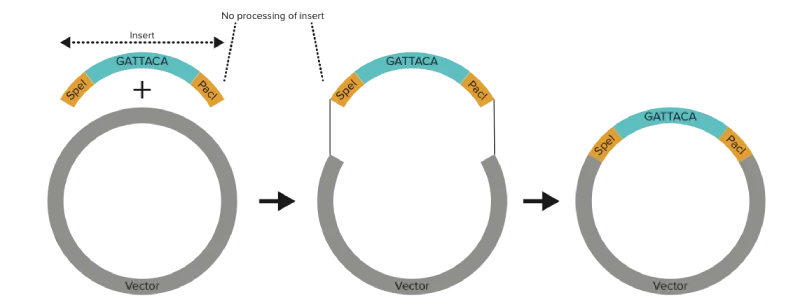
کلونینگ ژن با دقت بالا: جداسازی و انتقال ژن های خاص با دقت و کارایی بیشتر برای مطالعات ژنتیکی و کاربردهای درمانی.
تشخیص دقیق تر جهش ها و بیماری های ژنتیکی: شناسایی دقیق تر تغییرات در توالی DNA برای تشخیص و پیش آگهی بهتر بیماری ها.
مهندسی ژنتیک دقیق تر گیاهان و جانوران: ایجاد ارگانیسم های تراریخته با صفات دقیق و کنترل شده برای اهداف کشاورزی، دارویی و صنعتی.
زیست فناوری صنعتی: تولید محصولات و فرآورده های جدید با استفاده از آنزیم های محدود کننده مهندسی شده در شرایط extremophile.
پزشکی مولکولی: انتقال ژن های سالم به سلول های معیوب برای درمان بیماری های ژنتیکی با دقت و کارایی بیشتر.
چالش ها و ملاحظات
طراحی و سنتز آنزیم های جدید: فرآیندی پیچیده و چالش برانگیز است که نیاز به تخصص و دانش عمیق در زمینه های مختلف بیوشیمی، ژنتیک و مهندسی مولکولی دارد.
تضمین عملکرد و ویژگی های مطلوب: آزمایش و ارزیابی دقیق آنزیم های مهندسی شده برای اطمینان از عملکرد صحیح و دستیابی به ویژگی های مورد نظر ضروری است.
ملاحظات اخلاقی و زیست ایمنی: استفاده از آنزیم های مهندسی شده در زمینه های مختلف، نیازمند بررسی دقیق ملاحظات اخلاقی و زیست ایمنی برای جلوگیری از خطرات احتمالی است.
با وجود چالش ها، مهندسی آنزیم های محدود کننده افق های جدیدی را در زمینه تحقیقات ژنتیکی و کاربردهای مختلف آن می گشاید. این فرآیند نوآورانه، نویدبخش ابزارهای مولکولی قدرتمندتر، دقیق تر و کارآمدتر برای ارتقا سلامت انسان، توسعه پایدار و پیشرفت علمی در سال های آینده است.